ACSオメガ。 2023 8 月 23;8(35):32043-32052。土井: 10.1021/acsomega.3c03952。 eコレクション 2023 9 月 5.
PEG-メチルスルホンハイドロゲルの細胞適合性評価
要約
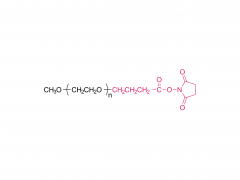
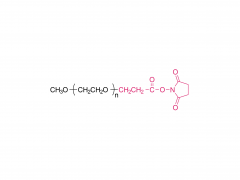
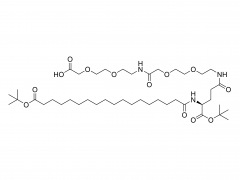
メチルスルホン誘導体化ポリ(エチレン)グリコール(PEG)マクロマーは、チオール化リガンドで生体官能化され、チオールベースの架橋剤で架橋されて、in situ 細胞カプセル化用の生物活性 PEG ハイドロゲルが得られます。メチルスルホニル チオール (MS-SH) 反応は、他のチオールベースの架橋システムと比較して、この目的に対していくつかの利点をもたらします。これらはカプセル化のために適切かつ調整可能な反応速度で進行し、良好な選択性で高い変換度に達し、安定した反応生成物を生成します。我々の以前の研究では、線維芽細胞と接触した架橋PEG-MS/チオールヒドロゲルの細胞適合性を実証しました。しかし、架橋部位で副生成物としてメチルスルフィン酸を生成する、in situ MS-SH 架橋反応自体の細胞適合性はまだ評価されていません。これらの研究は、これらのシステムの in vivo 応用の可能性を評価するために必要です。今回我々は、メチルスルホニル-チオール反応による in situ 架橋中の PEG ハイドロゲルの広範な細胞適合性研究を実行します。これらの結果を、細胞培養およびインビボ実験用に十分に確立されており、副産物の放出を伴わないマレイミドチオール架橋PEGと比較します。我々は、細胞層の上部でメチルスルホニルチオールゲルをその場で重合させた後でも、線維芽細胞と内皮細胞が生存し続けることを示します。細胞生存率は、マレイミド-チオール化学を使用してヒドロゲルをその場で架橋した後よりも優れているようです。内皮細胞の炎症誘発性表現型は低く、マレイミド-チオール反応によって得られるものと類似しています。最後に、単球の活性化は観察されません。全体として、これらの結果は、メチルスルホニル-チオールの化学反応が細胞適合性であり、内皮細胞および単球において高度な炎症促進反応を引き起こさないことを示しています。これらの結果により、メチルスルホニル チオールの化学は in vivo 試験に適格となり、将来的には最終的には臨床応用が可能となる [8]。
製品の詳細については、以下までお問い合わせください:
米国電話番号: 1-844-782-5734
米国電話番号: 1-844-QUAL-PEG
CHN 電話: 400-918-9898
電子メール: sales@sinopeg.com