I. 合成精度とデータ信頼性の向上
PROTAC分子の構築において、リンカーは不活性ではなく、そのわずかな変化が最終分子の性能に直接影響を与えます。従来の多分散PEGは、重合度の異なる分子の混合物です。これをリンカーとして使用すると、合成されるPROTACも実質的には混合物となります。これにより、2つの深刻な問題が発生します。1つ目は、ポリマー長の分布がバッチごとに変動するため、薬理学的データの再現が困難になることです。2つ目は、スクリーニングおよび最適化の過程で、観察された活性の変化がリンカー長の変化によるものか、混合物中の他の成分の干渉によるものかを確実に判別できないことです。
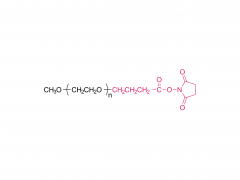
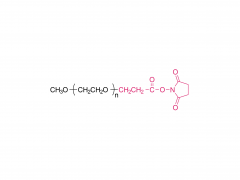
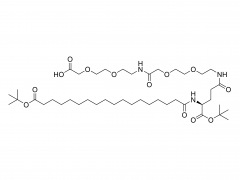
単分散PEG
この手法は、この問題を根本的に解決します。単一の明確な分子量を持つ分子で構成されているため、合成されるすべてのPROTAC分子は同一の構造と鎖長を持ちます。この絶対的な化学的均一性は、信頼性の高い構造活性相関(SAR)を確立するための基盤となります。研究者は、活性の増減が特定のリンカー長の寄与を直接反映していると確信でき、その結果、その後の薬剤最適化の取り組みを明確に導く、信頼性が高く再現性のある実験データが得られます。
II. 物理化学的および薬理学的特性の最適化
PROTAC分子は通常、リンカーで連結された2つの疎水性リガンドから構成されており、そのため水溶性が低く、生物学的実験において凝集または沈殿しやすいという問題があります。単分散PEG鎖は優れた親水性と柔軟性を備えています。これらをリンカーとして組み込むことで、PROTACの全体的な物理化学的特性を効果的に改善できます。「親水性ロープ」のように作用することで、疎水性リガンド部分の可溶化を促進し、PROTACの水溶性を高め、生理的条件下での凝集を防ぎます。
さらに、PEG鎖を導入することで、PROTACの生体内における薬物動態を調節することが可能です。分子量全体を増加させることで、腎濾過速度を低下させ、血中における薬剤の半減期を延長することができます。これにより、薬剤が標的組織に到達して効果を発揮する時間が長くなり、PROTACの生体内有効性の向上と投与レジメンの最適化に大きく貢献します。
III.生物活性の大幅な向上
PROTACの作用機序は、標的タンパク質とE3ユビキチンリガーゼへの同時結合によって安定な三元複合体を形成することに基づいている。このプロセスの効率は、リンカーの長さと形状が2つの「ハンドル」が最適に連携できるかどうかに大きく依存する。ここで用いられる単分散PEGリンカーは、「精密調節因子」として機能する。
PEG鎖の長さ(例えば、PEG2、PEG4、PEG6など)を精密に調整することで、2つのリガンド間の空間距離と相対的な配向を微調整し、安定な三元複合体を形成するための最適な形状を見つけることができます。この最適化の効果は大きく、多くの研究で、適切な単分散PEGリンカーを導入することで、PROTACの分解能(通常は半最大分解濃度DC50で測定)を数倍、あるいは10倍にも高め、最大分解率(Dmax)を90%以上にできることが確認されています。これは、適切に設計されたPEGリンカーによって、中程度の活性を持つ分子を強力かつ非常に効果的なタンパク質分解剤に変えることができることを示しています。
IV.医薬品スクリーニングおよび開発プロセスの加速
創薬の初期段階では、化学空間を迅速に探索し、最適な分子を特定することが極めて重要です。単分散PEGリンカーは、その明確な構造と固定された反応部位により、モジュール式のハイスループット合成戦略に非常に適しています。研究者は、レゴブロックで組み立てるように、異なる標的タンパク質リガンド、長さの異なる単分散PEGフラグメント、および異なるE3リガーゼリガンドを迅速に組み合わせることができます。この「プラグアンドプレイ」モデルにより、数百ものPROTAC分子を含む化合物ライブラリーを非常に短時間(例えば一晩)で構築することが可能になり、リード化合物の発見と最適化を劇的に加速させることができます。
単分散PEGの利点は、候補分子が初期スクリーニングから毒性試験、そしてプロセススケールアップへと進む過程でも持続します。合成経路と分析方法がミリグラムスケールからグラムスケールまで一貫しているため、開発中の技術移転が円滑に進み、研究室での発見から前臨床開発までの期間が大幅に短縮され、研究開発パイプライン全体の効率が向上します。