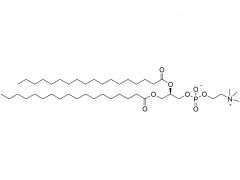
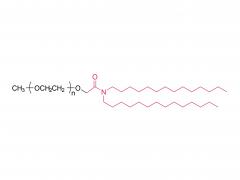
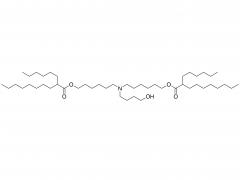
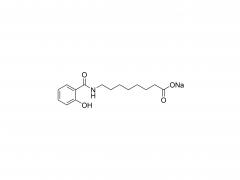
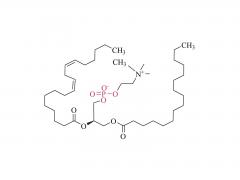
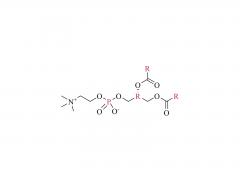
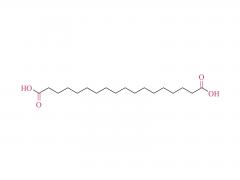
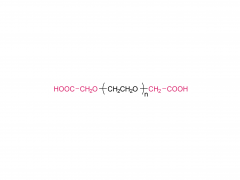
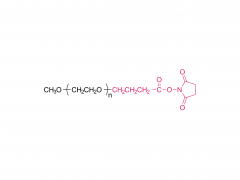
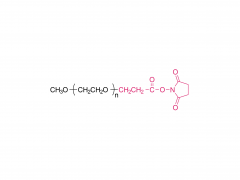
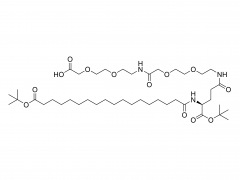
初公開日: 2020 年 5 月 27 日 https://doi.org/10.1002/macp.202000121 高い薬物負荷能力を示すコイル-g-ロッドグラフト共重合体から自己集合したルーズコアを持つ ミセル Qijing Huang、Zhanwen Xu、Chunhua Cai、Jiaping Lin 要約 高い薬物充填能力は、ミセル薬物送達ビヒクルの重要な要求の 1 つです。しかし、それは挑戦的な仕事です。本明細書では、ポリ(エチレングリコール)-グラフト-ポリ(γ-ベンジル-1-グルタメート)(PEG-g-PBLG)コイル-g-ロッドグラフトコポリマーから自己集合したミセルが、ドキソルビシン (DOX) モデル薬。実験と散逸粒子動力学シミュレーションを組み合わせた研究によって明らかになったように、ミセルの高い薬物担持能力は、ミセルの緩いコア構造に関連しています。これらのミセルでは、疎水性 PBLG グラフトは、その剛直な性質とグラフトコポリマーのコイル-g-ロッドトポロジーによりミセルコア内にランダムに分散し、その結果ミセルのコアが緩くなります。ロッドグラフトの長さ、コイルバックボーンの長さ、ミセルコア内のロッドグラフトの配置に影響を与えるロッドグラフトのグラフト率などのグラフトコポリマーの構造は、ミセルの薬物担持能力に影響を与えます。 。さらに、グラフトコポリマーとDOXの間の強いπ-πスタッキング相互作用も、高い薬物担持能力を達成する上で重要な役割を果たしています。 in vitro 研究では、これらの薬物を封入したミセルが良好な生体適合性を示し、DOX がミセルから徐々に放出されることが明らかになりました。 関連製品 略称: PEG-g-NH2 名前:ポリ(エチレングリコール) グラフト アミン 製品の詳細については、以下までお問い合わせください: US Tel: 1-844-782-5734 US Tel: 1-844-QUAL-PEG CHN Tel : 400-918-9898 電子メール: sales@sinopeg.com
もっと見る